Церебральная ишемия у новорождённых детей
Ишемия – это нарушение проходимости сосудов. При сужении протока мозг недополучает питательные вещества и кислород, снижаются функции жизненно важных систем. Если кислородное голодание клеток продолжается продолжительный период, развиваются тяжелые осложнения. Это одна из распространенных причин инвалидности при детском церебральном параличе.
Среди внутриутробных причин ишемии у грудничка:
- отслойка или незрелость плаценты;
- отсутствие родовой деятельности после отхождения вод;
- обвитие пуповиной;
- врожденные аномалии артерий мозга;
- прием беременной наркотиков или злоупотребление алкоголем;
- перенесенные будущей матерью инфекции;
- наследственный фактор;
- анемия.

После родоразрешения кислородное голодание чаще возникает у недоношенных детей. Предрасполагающими факторами становятся:
- открытое овальное окно в сердце;
- заражение крови в первые дни после родов;
- врожденные аномалии печени, селезенки, костного мозга.
Важно!
Среди факторов риска, влияющих на формирование церебральной ишемии у новорожденных, выделяют: возраст роженицы старше 35–40 лет, многоплодную беременность, гестоз на позднем сроке.
Симптомы заболевания
Характерные признаки церебральной ишемии проявляются в течение 1–3 суток после рождения. Около 70% малышей получают патологические изменения во время внутриутробного развития. У 20% маленьких пациентов поражение мозга развивается во время тяжелых и травматичных родов. В зависимости от тяжести состояния выделяется несколько степеней болезни.
Симптомы 1-й степени

Начальная стадия проявляется в период 7–10 суток после появления на свет. При правильной диагностике и быстром начале лечения врачам удается минимизировать последствия для ЦНС. Церебральная ишемия 1-й степени у новорожденных характеризуется следующими особенностями:
Читайте также:
- малыш беспокоен, капризен из-за сильных головных болей, сосудистых спазмов;
- наблюдается тонус мышц нижних и верхних конечностей;
- плохой аппетит;
- выраженный коленный рефлекс.
На этом этапе сложно правильно поставить диагноз, поэтому требуется постоянный контроль неонатолога и невропатолога, ряд анализов и диагностических процедур.
Симптомы 2-й степени

Опытный специалист может выявить церебральную ишемию 2-й степени у новорожденных уже на 1–2-е сутки по характерным признакам:
- появляются приступы остановки дыхания во время глубокой фазы сна. Ребенок просыпается при попытке вдохнуть, синеет носогубный треугольник. Состояние продолжается 15–20 секунд.
- Мышечный тонус снижен, коленный рефлекс выражен слабо.
- Кожные покровы становятся бледными, выделяется рисунок кровеносных сосудов.
- При ишемии головного мозга у новорожденного может повышаться внутричерепное давление, возникает отечность и признаки гидроцефалии. В этом случае голова имеет непропорциональные размеры и форму.
Степень развития 2-й стадии оценивается по угнетению безусловных рефлексов. Младенец плохо глотает материнское молоко или смесь, не удерживает палец родителя. При отсутствии лечения и реабилитации состояние только усугубляется: появляются головные боли, нарушается координация движений, способность разговаривать и решать логические задания.
Симптомы 3-й степени

При длительном кислородном голодании нейроны погибают, нарушается структура мозгового вещества. Если некроз захватывает большие участки, симптоматика при церебральной ишемии 3-й степени крайне тяжелая:
- выраженная аритмия или тахикардия;
- повышенное внутричерепное давление;
- практически полное отсутствие глотательного рефлекса;
- неподвижность из-за сниженного мышечного тонуса;
- отсутствие реакции на любые раздражители (громкие звуки, свет, голос родителей);
- спазмы мускулатуры лица, судороги конечностей;
- продолжительные обмороки.
При третьей степени нередко наблюдаются ишемия сердца, нарушение функций почек, кишечника, органов дыхания. Ребенок отстает в росте и весе, страдает от пареза конечностей или полного паралича. Это становится причиной тяжелой формы ДЦП или ранней смертности.
Методы диагностики
Церебральная ишемия у детей грудного возраста – сложный диагноз, который требует комплексного обследования разными способами. После рождения дети с нарушениями мозгового кровообращения попадают под круглосуточный контроль: нередко происходит обострение, наступает глубокий обморок или кома. Помогают подтвердить заболевание следующие анализы и методы исследования организма:
- Первичный осмотр. Проводит неонатолог непосредственно в родильном зале. На основании нескольких показателей он выставляет оценки по шкале Апгар. У детей с кислородным голоданием они диагностируются на низком уровне. Врач определяет наличие основных рефлексов, мышечного тонуса и попытки самостоятельного дыхания.
- Анализы. Перед назначением лечения младенцу проводят общий и биохимический анализ крови, оценку свертываемости, количества углекислого газа.
- МРТ головного мозга. Если у грудничка возникают судороги, потеря сознания и другие признаки тяжелого поражения, проводят компьютерное сканирование. На срезах можно увидеть участки некроза, состояние кровеносных сосудов, гематомы.
- УЗИ мозга. Диагностическая процедура рекомендуется для определения внутричерепного давления, оценки состояния коры и мозгового вещества.
- ЭЭГ. Электроэнцефалограмма обязательно проводится при подозрении на церебральную ишемию у детей. Безболезненный способ помогает обнаружить причину судорог, потери сознания, подобрать оптимальную терапию.
Информация!
Читайте также:
При необходимости используется ЭКГ, рентген и ангиография для выявления врожденных патологий кровеносной системы, опухолей или аневризмы.
Лечение церебральной ишемии
При легкой степени терапия начинается с массажа. Он помогает снять тонус мышц, улучшает кровообращение и обладает общеукрепляющим эффектом. Воздействие на биологически активные точки стимулирует развитие сенсорных зон. Терапия дополняется регулярными прогулками на свежем воздухе, успокаивающими ванночками, полноценным питанием, обогащенным витаминами.
При средней и тяжелой степени лечение рекомендуется в условиях стационара. Оно сочетает несколько методов:
- Интубация в 1–2-е сутки для предотвращения остановки дыхания, улучшения кровоснабжения головного мозга. При необходимости грудничка переводят на аппарат ИВЛ.
- При обнаружении тромба проводят медикаментозное лечение с помощью разжижающих препаратов. После удаления восстанавливается стабильный кровоток, улучшается общее состояние малыша. При необходимости удаляют сгусток хирургическим путем.
- Ежедневный прием противосудорожных препаратов, стимулирующих улучшение мышечного тонуса.
- Введение лекарств для поддержки сердечной мышцы, нормализации ритма и давления.
Повышенное внутричерепное давление создает угрозу для жизни и здоровья. Возникает отечность в подкорковом слое, которая ухудшает состояние и ускоряет гибель нейронов. Если проблема выражена в легкой форме, используют мочегонные препараты. При тяжелой стадии рекомендуется установка специального шунта. Миниатюрная трубка отводит излишнюю жидкость в мочевой пузырь или брюшную полость, помогая снизить остроту проблемы. По мере роста малыша она заменяется подходящей по размеру.
Среди современных методов выделяется гипертермия. Это искусственное понижение температуры тела на несколько градусов, при котором замедляются основные процессы. Так удается остановить гибель нейронов мозга и предотвратить летальные последствия. При дальнейшей реабилитации реконвалесцента используются электрофорез, магнитотерапия, лечебная гимнастика, гидротерапия.
Перечень последствий, вызываемых заболеванием
При своевременном лечении можно уменьшить проявления болезни. Первая степень хорошо реагирует на терапию, зачастую проходит без следа через 10–12 месяцев. В редких случаях негативные последствия проявляются в школьном возрасте в виде неусидчивости, рассеянности и гиперактивности. В переходном периоде могут беспокоить мигрень, метеочувствительность.
Вторая степень заболевания
Последствия церебральной ишемии у новорожденных при диагностике 2-й степени зависят от многих факторов, уровня повреждения центральной нервной системы. Среди распространенных проблем:
- предрасположенность к аутизму;
- задержка речевого и психического развития;
- хроническая бессонница;
- синдром дефицита внимания;
- замкнутость при общении со сверстниками;
- заикание;
- приступы мигрени;
- нарушения психики;
- плохая успеваемость в школе.
Важно!
У детей, перенесших кислородное голодание, повышается риск эпилепсии, заболеваний сердечно-сосудистой системы. Для устранения последствий рекомендуется проведение реабилитации под контролем невропатолога.
Читайте также:
Третья степень
При тяжелой форме заболевания каждый второй малыш погибает в течение месяца после родов от врожденных патологий или инфекций. У 80% детей некроз затрагивает наиболее важные центры, поэтому последствия необратимы. Впоследствии диагностируется детский церебральный паралич, психические отклонения, могут полностью отсутствовать речь и двигательная активность. Только у 1 из 10 малышей отклонения незначительны, постепенно исчезают по мере взросления.
Профилактика ишемии
Уменьшить риск развития церебральной ишемии поможет соблюдение простых рекомендаций врачей:
- отказ от курения до зачатия;
- своевременное лечение простуды и инфекций при беременности;
- регулярное выполнение УЗИ и скрининга;
- умеренные физические нагрузки;
- мониторинг артериального давления;
- полноценный отдых ночью и дневной сон;
- прием витаминных комплексов.
Женщине необходимо регулярно сдавать анализы, отслеживать уровень гемоглобина. Чтобы плод получал больше кислорода, гинекологи советуют будущим мамам чаще бывать на свежем воздухе, правильно питаться, обязательно следить за набором веса.
Если заболевание диагностировано, необходимо как можно быстрее приступать к лечению, внимательно соблюдать все предписания врачей. У детей младшего возраста нервные клетки сохраняют способность регенерировать, восстанавливать связи. Поэтому прогноз зависит от стадии болезни, области поражения и компетентности невролога.
Врожденные пороки сердца
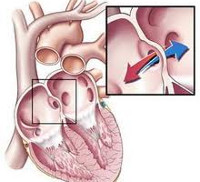
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
- Причины врожденных пороков сердца
- Классификация врожденных пороков сердца
- Нарушения гемодинамики при врожденных пороках сердца
- Симптомы врожденных пороков сердца
- Диагностика врожденных пороков сердца
- Лечение врожденных пороков сердца
- Прогноз и профилактика врожденных пороков сердца
- Цены на лечение
Общие сведения
Врожденные пороки сердца — весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).

Врожденные пороки сердца
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
Ввиду особенностей антенатальной гемодинамики, кровообращение развивающегося плода при врожденных пороках сердца, как правило, не страдает. Врожденные пороки сердца проявляются у детей сразу после рождения или через какое-то время, что зависит от сроков закрытия сообщения между большим и малым кругами кровообращения, выраженности легочной гипертензии, давления в системе легочной артерии, направления и объема сброса крови, индивидуальных адаптационных и компенсаторных возможностей организма ребенка. Нередко к развитию грубых нарушений гемодинамики при врожденных пороках сердца приводит респираторная инфекция или какое-либо другое заболевание.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой — электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Источник https://arhmedlab.ru/info/tserebralnaya-ishemiya-u-novorozhdyonnyh-detej
Источник https://www.krasotaimedicina.ru/diseases/zabolevanija_cardiology/congenital-heart-defect
Источник