«Пятьдесят лет с ВИЧ». Насколько человечество близко к исцелению?
Никто не знал, что убило Роберта Рейфорда. Афроамериканскому мальчику было всего 15, когда он оказался в городской больнице Сент-Луиса в конце 1968 года, и медики не смогли понять, что с ним.
Необъяснимая опухоль в районе гениталий быстро распространилась по всему телу Рейфорда. Хламидии, обычно локализующиеся в области заражения, циркулировали по его кровеносной системе. Мелкая пурпурная сыпь на внутренней стороне бедра подсказывала, что это рак, но такую форму обычно встречали только у пожилых евреев-ашкенази и итальянцев, а не у чернокожих подростков, никогда не покидавших Миссури.
Мальчик почти не разговаривал на протяжении 18 месяцев, пока его лечили в трех разных больницах. «Он был типичным 15-летним подростком, который не собирается откровенничать со взрослыми, особенно учитывая, что я белый, а он черный», — два десятилетия спустя расскажет St Louis Post-Dispatch один из его докторов. Рейфорд признался, что у него был секс с соседской девушкой, но мало что рассказал свыше того.
по теме

Общество
Цветные женщины: стареющие, невидимые, ВИЧ-позитивные
Пневмония прервала короткую жизнь Рейфорда ночью 15 мая 1969 года, но его тело сдалось еще раньше — болезни, с которыми здоровый организм способен справиться, не встречали в нем сопротивления. Врачи, озадаченные его смертью, убедили родственников отдать тело на аутопсию и сохранили образцы для исследований в будущем.
Двенадцать лет спустя, в 1981 году, всплыли сообщения о молодых людях, умирающих от агрессивных форм пневмонии. У многих замечали черно-красную сыпь, схожую с той, что обнаружили на внутренней стороне бедра Рейфорда. Большинство из них оказались гомосексуалами, и (как и у Рейфорда) у многих была настолько дисфункциональная иммунная система, что обычная простуда могла привести к госпитализации. У них был СПИД, от которого не существовало лечения.
В середине 80-х молодой ретровирусолог, работавший в Тулейнском университете в Новом Орлеане, протестировал образцы, взятые из тела Рейфорда. Они «содержали антитела ко всем девяти белкам ВИЧ, использованным в тесте», — результаты опубликовали в Chicago Tribune в 1987 году. Мать Рейфорда Констанция едва ли могла прокомментировать эту новость, когда репортеры появились на ее пороге: «Ему было всего 16 лет», — сказала она, смущенная и заметно расстроенная посмертной славой ее сына.
Это открытие доказало, что СПИД появился в США более чем на десятилетие раньше, чем предполагали популярные теории, и отвело Рейфорду сомнительное место в истории ретровируса, который с тех пор убил порядка 35 миллионов людей во всем мире.

Резервуары и недобитые вирусы
В США СПИД обосновался и распространился среди определенных групп людей, которые потом стали называть «уязвимыми»: наркопотребителей, секс-работниц, гомо- и бисексуальных мужчин, а также афроамериканцев. Болезнь убила целое поколение творческих людей, таких как художник Кит Харинг, фотограф Питер Худжар, актер Дэвид Войнарович, пионер танцевальной сцены Уилли Нинджа и голливудская звезда Рок Хадсон. Но больше всего людей погибло в тропической Африке, где слабая система здравоохранения, а также стигма вкупе с религиозным противостоянием раздаче презервативов помогли вирусу распространиться как лесной пожар, убивая миллионы людей.
Через пятьдесят лет после смерти Рейфорда информация о том, что четвертый пациент, предположительно, исцелилися от ВИЧ, вызывает надежду. Современная антиретровирусная терапия подавляет вирусную нагрузку до неопределяемого уровня, а это значит, что человек не может никому передать вирус, кроме того, продолжительность жизни человека с ВИЧ ничем не отличается от жизни без заболевания. И все же «Лондонский пациент», который живет без ВИЧ уже 21 месяц, дает надежду на нечто большее — на исцеление.
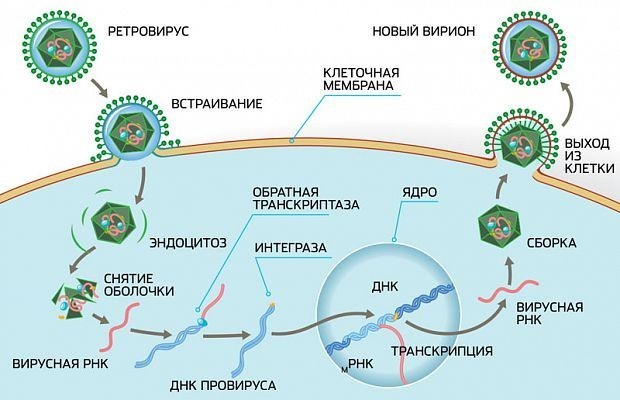
Человеческое тело способно побороть большинство вирусов, но вирус иммунодефицита поражает и уничтожает именно те клетки, которые нужны, чтобы его убить. Они называются CD4-лимфоциты (особая разновидность T-лимфоцитов, несущая на себе рецептор CD4, к которому впоследствии и прикрепляется ВИЧ, перед тем как попасть в клетку) и ответственны за координацию иммунного ответа организма. Заражая CD4-лимфоциты, вирус взламывает их внутреннее устройство и начинает создавать тысячи своих копий, которые, как споры, разлетаются по кровотоку. Соответственно, инфицируется еще больше клеток, а цикл повторяется раз за разом. Организм, пытаясь сдержать вирус, убивает зараженные клетки. «После того, как CD4+ Т-клеток не осталось, у вашей иммунной системы нет штурвала», — объясняет доктор Карл Диффенбах, директор Отделения СПИДа Национального института изучения аллергий и инфекционных заболеваний США.
по теме

Общество
Как отбеливают историю ВИЧ: смерть чернокожего подростка от СПИДа в 1969 году
Антиретровирусная терапия спасла миллионы жизней, не позволяя вирусу размножаться, а клеткам иммунитета помогла восстанавливаться, но она не может до конца удалить вирус из организма. Проблема в том, что, когда ВИЧ попадает в клетку, он интегрирует свой РНК в ДНК клетки-хозяина и таким образом прячется в различных уголках организма, оставаясь незаметным для иммунной системы. Он скрывается в так называемых «резервуарах», которые просто не могут «добить» лекарства, но если их перестать принимать, то вирус ничто не будет ограничивать, и он сможет без объявления войны развернуть полномасштабное наступление. «Все, что вам нужно, — это один нетронутый вирус, спрятавшийся в CD4-клетке, и в какой-то момент он проснется и распространится», — рассказывает Диффенбах.
Редкая мутация и опасная процедура
Однако 5 марта этого года было объявлено о прорыве в медицине: команда ученых в Великобритании успешно вылечила от ВИЧ-инфекции человека, известного под кодовым именем «Лондонский пациент», на тот момент у него была ремиссия на протяжении 18 месяцев. Ему поставили диагноз ВИЧ в 2003 году, а в 2012 году к этому добавилась генерализованная лимфома Ходжкина — рак лимфатической системы. Единственным возможным способом лечения осталась интенсивная химиотерапия, за которой последовала трансплантация костного мозга, содержащего стволовые клетки, необходимые, чтобы восстановить очищенную иммунную систему. Эта процедура предоставляла возможность исцелить Лондонского пациента и от ВИЧ.
Ученые выбрали донора с редкой генетической мутацией — устойчивостью к ВИЧ. Чтобы вирус иммунодефицита попал в клетку, ему необходимо прикрепиться к белку CCR5, находящемуся на поверхности самой клетки. А мутация как раз меняет форму этого белка, не позволяя вирусу закрепиться и проникнуть внутрь.
Иммунная система Лондонского пациента была восстановлена с помощью таких устойчивых к заражению клеток, тем самым ВИЧ был полностью удален из его организма.
«Наконец! У кого-то же должно было получиться!» — отреагировал на новость Диффенбах. Такая процедура сработала всего несколько раз, причем первым был Тимоти Рэй Браун, которого еще называют «Берлинским пациентом». Он находится в ремиссии уже более 10 лет.
Но лечение Брауна было гораздо серьезнее: он пережил облучение всего тела и две пересадки стволовых клеток, каждая из которых смертельно опасна, если клетки не приживутся. Были случаи, когда несколько пациентов, прошедших через подобное, умерли: из-за рецидивов рака, самой процедуры трансплантации, либо снова заболели ВИЧ.
«Берлинский пациент заставил нас задуматься, должен ли пациент побывать на грани смерти, чтобы исцелиться от ВИЧ, — рассказывает профессор Равиндра Гупта, руководивший командой Лондонского пациента. — Теперь мы знаем, что нет. Можно использовать менее токсичную химиотерапию. Возможно, риски можно сократить еще больше». Однако он предупреждает: уменьшение вреда от процедуры не означает, что она станет безопасной или эффективной.
Во-первых, ее слишком опасно назначать людям, получающим антиретровирусную терапию и уже ведущим здоровую жизнью. Во-вторых, трансплантация стволовых клеток связана с риском: когда клетки не приживаются, тело бунтует и даже может убить пациента. И, в-третьих, для процедуры нужно найти донора с мутацией CCR5, также имеющего сходный с пациентом состав крови. А это крайне редкая комбинация факторов.
Для Гупты главный итог эксперимента с Лондонским пациентом — не столько сама операция, сколько подтверждение идеи, что через работу с CCR5 можно излечиться от ВИЧ. Он считает, что самый очевидный способ использования этого открытия — редактирование генов. Хотя изменение генома человека в профессиональном сообществе вызывает дискуссии, в том числе и с этической точки зрения.

Так, в ноябре 2018 года стало известно, что в Китае рождены генетически модифицированные девочки-близнецы. Их особенность — врожденный иммунитет против ВИЧ-инфекции. Эксперимент провел профессор Хэ Цзянькуй из Южного университета науки и технологий в Шэньчжэне.
После обнародования этой информации в мировом научном сообществе разгорелся скандал: более ста ученых подписали письмо, осуждающее «безрассудные эксперименты» над человеческими генами, а власти Китая были вынуждены инициировать расследование деятельности генетика. Позже появилась информация о том, что Хэ может грозить смертная казнь, но не за сами опыты, а за взяточничество и коррупцию.
Но Гупта ищет иные варианты генных модификаций. Редактирование генов эмбрионов влияет на все клетки будущего взрослого, и эти изменения передаются будущим поколениям. Но редактирование клеток взрослого не приводит к таким последствиям. Главная проблема — убедиться в аккуратности процедуры. Кроме того, потребуются десятилетия, если это вообще возможно, чтобы сделать эту процедуру более простой.
«Пнуть и убить»
Сейчас в научном мире одновременно разрабатывается еще несколько стратегий, и в этом году две из них попали в новости. Первая использует антитела — белки, которые иммунная система вырабатывает для борьбы с различными инфекциями. Как и в случае с Лондонским и Берлинским пациентами, этот метод подходит людям с врожденным иммунитетом к ВИЧ — их еще называют «элитными» контроллерами. В их организме образуются антитела, способные нейтрализовать ВИЧ, останавливая продвижение вируса, когда он перемещается между клетками.
Наука и технологии против ВИЧ: пять основных трендов

Среди нас живут 1,1 млн ВИЧ-позитивных россиян. Вместе в ростом инфицированных растет и смертность. РБК Тренды и Фонд «СПИД.ЦЕНТР» рассказывают, как новые методы лечения ВИЧ помогают снизить смертность и продлить жизнь
Согласно данным ФБУН Центрального НИИ эпидемиологии Роспотребнадзора, Федерального научно-методического центра по профилактике и борьбе со СПИДом, ВИЧ-инфекция вышла за пределы уязвимых групп населения и активно распространяется в общей популяции. Большинство пациентов, впервые выявленных в первом полугодии 2021 года, инфицировались при гетеросексуальных контактах (67,3%). Количество инфицированных при половых контактах ежегодно увеличивается. В первом полугодии 2021-го зарегистрировано три случая подозрения на инфицирование ВИЧ, связанное с оказанием медицинской помощи, и один случай инфицирования ВИЧ ребенка при оказании медицинской помощи за пределами России.
Почему ВИЧ сложно лечить
Вирус иммунодефицита человека (ВИЧ) вызывает хроническое инфекционное заболевание, прогрессирующее без лечения. Это один из уникальных вирусов, которые поражают клетки иммунной системы — так называемые CD4+ Т-лимфоциты, функция которых состоит в распознавании и уничтожении чужеродных для организма агентов. Вирус как «троянский конь» встраивается в геном иммунных клеток и блокирует все средства их защиты, избегая обнаружения иммунной системой. Антитела против ВИЧ вырабатываются, но они не способны остановить этот процесс. Без лечения ВИЧ-инфекция медленно прогрессирует, истощая иммунную систему организма. Через 5–10 лет после инфицирования начинается стадия вторичных проявлений, когда у ВИЧ-положительного развиваются другие сопутствующие заболевания.
Профилактика: значимое снижение рисков инфицирования ВИЧ
- Доконтактная профилактика
Доконтактная профилактика (ДКП или PrEP) — это прием неполной схемы тех же препаратов, которые принимают люди, живущие с ВИЧ: сочетания тенофовир + эмтрицитабин или тенофовир + ламивудин.
Если препараты ДКП успели попасть в организм заранее, то при проникновении в него вируса вещества ДКП убивают ВИЧ еще до того, как тот успеет закрепиться в теле человека. Препараты нужно принимать ежедневно в одно и то же время.
Защита, которую обеспечивает PrEP при правильном приеме таблеток, — почти 100%. Требуется консультация и контроль врача.
В экстренных случаях, когда есть риск заболевания после незащищенного контакта с инфицированным, используют постконтактное лечение (ПКП, PEP). Это месячный курс терапии. При быстром начале лечения в течение первых 24–72 часов есть высокие шансы избежать инфицирования. Но эти шансы никогда не равны 100%.
Лечение ВИЧ: антиретровирусная терапия
Основной способ взять ВИЧ-инфекцию под контроль — антиретровирусная терапия. Она включает в себя препараты, останавливающие жизненный цикл ВИЧ на разных этапах.
Антиретровирусная терапия меняет качество жизни пациентов с ВИЧ:
- останавливает размножение вируса;
- позволяет иммунной системе самой восстановиться;
- предотвращает передачу ВИЧ половому партнеру;
- позволяет женщине родить детей без вируса.
Ученые доказали, что ВИЧ-положительный человек, принимающий эффективную терапию, не может передать вирус при незащищенных сексуальных контактах.
Сегодня в России зарегистрировано более 20 препаратов из шести разных классов антиретровирусной терапии. Для каждого пациента подбирается комбинация, которая будет эффективна и не вызовет побочных эффектов.
Терапия ВИЧ сильно изменилась: первые схемы лечения предполагали многократный прием достаточно токсичных препаратов, что породило миф о том, что «таблетки убивают быстрее, чем ВИЧ». В настоящее время лекарства принимаются один, реже — два раза в сутки, схемы лечения включают от одной до шести таблеток.
Прорыв 2021 года в лечении ВИЧ — регистрация первых инъекционных форм антиретровирусной терапии на рынках Канады, США и Европы. В ближайший год эта форма должна появиться в России. Исследования доказали эффективность терапии при однократных инъекциях каждые 1–2 месяца (вместо ежедневного приема терапии). Следующее поколение лечения — инъекционный препарат с введением один раз в полгода. Потенциально эти же лекарства можно будет использовать для снижения риска инфицирования с той же продолжительностью действия.
Исследования новых методов лечения ВИЧ: генетические ножницы
Пока излечиться от ВИЧ невозможно. Основной причиной, почему ВИЧ-инфекция до сих пор остается неизлечимой, несмотря на наличие препаратов антиретровирусной терапии, — недоступность для воздействия медикаментов на те копии вируса, которые прячутся в «спящих» клетках, в так называемых резервуарах ВИЧ, одним из которых является костный мозг человека.
Известные случаи излечения от ВИЧ связаны с пересадкой костного мозга от доноров с мутацией генов CCR5, делающих носителей этой мутации неуязвимыми для ВИЧ. В настоящее время ученые отслеживают состояние еще 38 пациентов с ВИЧ, которым был трансплантирован устойчивый к вирусу материал.
Этот метод не может быть масштабирован по двум причинам: ущерб для здоровья от трансплантации несоизмеримо выше, чем от ВИЧ-инфекции (излечившиеся пациенты проходили процедуру не в связи с ВИЧ, а из-за онкологических заболеваний), а сама мутация не может служить надежной защитой перед быстро мутирующим вирусом, новые штаммы которого могут стать невосприимчивы к этой естественной защите.
Тем не менее случаи излечения именно этим путем создали значительное поле для исследований: на их основе появились как возмутивший общественность эксперимент на генетически модифицированных детях, итог которого общественности неизвестен, так и испытание метода редактирования гена CCR5 в организме живого человека, которое завершатся в Санкт-Петербурге в 2022 году.
Одна из надежд на излечение от ВИЧ связана с методом «генетических ножниц» CRISPR, с помощью которых можно «вырезать» в живых клетках участки ДНК, модифицированные вирусом для собственного размножения. В настоящее время большинство разрабатываемых методов борьбы с ВИЧ использует стратегию «shock and kill» — реактивацию вируса и его уничтожение. Существует другая изучаемая стратегия — «block-lock-excise», то есть уничтожение латентного вируса без реактивации: напротив, предполагается «запереть» вирус в спящих клетках, после чего удалить из организма с помощью технологии CRISPR-Cas9.
Разработки вакцин от ВИЧ
Эффективной вакцины против ВИЧ не существует — пока.
За все время в клинических исследованиях испытывали более 40 вакцин. Максимальный эффект в сокращении новых случаев ВИЧ — только 25%. Созданию вакцины препятствует особенность жизненного цикла ВИЧ и его высокая изменчивость — особенно его внешней оболочки. Это позволяет вирусу быстро обходить искусственный иммунитет.
Продолжается исследование бельгийской вакцины Mosaico. В 2022 году планируется публикация исследования перспективной кадидатной вакцины HIVconsvX от Оксфордского университета.
Еще одну надежду на вакцинацию «подарила» пандемия коронавируса: в ходе поиска подходов к ее профилактике начали использовать технологию мРНК-вакцины. В текущем году стало известно о запуске испытаний мРНК кандидатных препаратов против ВИЧ от американской компании Moderna.

К сожалению, разработка российских вакцин против ВИЧ началась только в 1997 году, и из-за проблем с финансированием многократные попытки по созданию вакцин в РФ ни разу не были доведены до конца. В 2020 году разработками занимались в Петербурге — ГосНИИ ОЧБ и «Биомедицинский центр» (ДНК-вакцина). Также на базе Московского городского центра профилактики и борьбы со СПИДом тестировали терапевтическую вакцину, позволяющую носителю жить без терапии в течение длительного времени.
Диагностика: шесть видов анализов
Рынок средств диагностики ВИЧ активно растет. Согласно исследованию американского агентства GMI, к 2024 году объем мирового рынка средств диагностики ВИЧ превысит $5 млрд.
Диагностика включает скрининг и подтверждающие тесты для проверки на заболеваемость ВИЧ-1, 2 и группы О. Эти тесты имеют основное применение для скрининга и дифференциации различных групп и подтипов вируса иммунодефицита человека. Благодаря технологическому развитию стали доступны экспресс-тесты на уровень клеток CD4, нуклеиновые кислоты NAT, антиген p24 и диагностика для новорожденных EID.
Антитела к ВИЧ появляются после начала активного размножения вируса. Они обычно обнаруживаются в сыворотке крови через 6–12 недель после инфицирования. Тесты на антитела ВИЧ высоко надежны при относительно низкой стоимости.
При определении антигена p24 в крови ВИЧ-инфекция может быть выявлена раньше, чем традиционными тестами для определения антител. Тесты на антиген имеют низкую чувствительность. Они не дают ложноположительных результатов, но возможны ложноотрицательные. То есть отрицательный результат не исключает инфицирование, а положительный — подтверждают с помощью тестов на антитела. Тест на антиген p24 всегда применяется вместе с тестами на антитела.
- Тесты на ВИЧ четвертого поколения
В тестах четвертого поколения объединили разные технологии, чтобы обнаружить как антиген p24, так и антитела. Тесты четвертого поколения менее дорогие, чем NAT. Широко распространены в России.
- Тесты на нуклеиновые кислоты (NATNAAT)
Положительные результаты теста на NAT дополнительно подтверждают тестированием на антитела к ВИЧ. Тесты NAT стоят дорого и поэтому используются в особых случаях — для обнаружения ВИЧ у новорожденных и в банках крови. Тесты NAT не зарегистрированы в РФ.
Определяет наличие и количество ВИЧ в миллилитре крови и других биологических жидкостях. Имеет высокую точность и стоимость, для скрининга не применяется. Используется для определения вирусной нагрузки у ВИЧ-положительных пациентов.
Этот тест не выявляет ВИЧ, а служит для измерения уровня клеток CD4 или Т-лимфоцитов — показатели, важные для для качества жизни пациентов с ВИЧ. Это белые клетки крови, предназначенные для распознавания болезнетворных организмов в нашем теле, которые должны уничтожаться иммунной системой. Снижение уровня CD4-клеток ниже 200 означает очень серьезные нарушения иммунной системы.
Эпидемия ВИЧ началась раньше пандемии коронавируса. Согласно UNAIDS, в 2020 году во всем мире насчитывалось не менее 37,6 млн пациентов с ВИЧ. Но главный тренд — за последние десятилетия инновации существенно изменили качество и продолжительность их жизни, а доступность диагностики и лечения снизили смертность на 61% по сравнению с максимумом в 2004 году. Также с 1996 года более чем на 30 лет выросла общая продолжительность жизни человека с ВИЧ при условии раннего обнаружения и использования терапии.
Подробнее о подходах к лечению и о том, как инновации продолжают улучшать качество жизни с ВИЧ, расскажут ученые-медики из разных стран на онлайн-конференции PROHIV 2021, которая пройдет 20–21 сентября.
Источник https://spid.center/ru/articles/2472
Источник https://trends.rbc.ru/trends/social/613b11ee9a79473d438c0f62
Источник