Псевдомембранозный колит
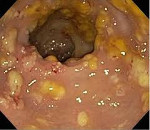
Псевдомембранозный колит – это острое воспаление толстого кишечника, вызываемое условно патогенными клостридиями и возникающее на фоне приема антибиотиков или (реже) других лекарственных средств. Клинические проявления могут варьировать. Обычно выявляются боли в животе и продолжительная диарея в сочетании с признаками общей интоксикации. В тяжелых случаях возможны грубые повреждения кишечной стенки, выраженные расстройства обмена и летальный исход. Заболевание диагностируется на основании симптомов, данных осмотра, анализов крови и кала, эндоскопического исследования. Лечение – отмена антибиотика, диета, этиотропная терапия, коррекция обменных нарушений.
МКБ-10
K52.8 Другие уточненные неинфекционные гастроэнтериты и колиты
- Причины
- Симптомы колита
- Диагностика
- Лечение псевдомембранозного колита
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Псевдомембранозный колит – тяжелое осложнение приема антибиотиков, реже лечения препаратами других групп, в результате которого у больного развивается специфический дисбактериоз, сопровождающийся воспалением толстого кишечника с образованием характерных пленок на слизистой оболочке. Дисбактериоз и воспаление слизистой вызывают анаэробные грамположительные бактерии Clostridium difficile. В тяжелых случаях псевдомембранозный колит сопровождается выраженной интоксикацией, повреждениями стенки кишечника вплоть до перфорации, общей дегидратацией и грубыми электролитными расстройствами, нередко – в сочетании нарушениями белкового обмена. Возможен летальный исход. Лечение осуществляют специалисты в области клинической проктологии и гастроэнтерологии.

Псевдомембранозный колит
Причины
Причиной псевдомембранозного колита является нарушение нормальной кишечной микрофлоры, сопровождающееся избыточным размножением условно патогенной бактерии Clostridium difficile. В подавляющем большинстве случаев дисбактериоз, предшествующий развитию псевдомембранозного колита, возникает на фоне приема антибиотиков, однако в отдельных случаях состав микрофлоры кишечника может меняться под влиянием цитостатиков, иммуносупрессоров и слабительных средств.
Чаще всего псевдомембранозный колит вызывают такие антибиотики, как клиндамицин, амоксициллин, ампициллин, линкомицин и препараты из группы цефалоспоринов. Реже псевдомембранозный колит развивается при приеме левомицетина, эритромицина, тетрациклина и пенициллина. Из-за подавления микробов-симбионтов в кишечнике начинают размножаться Clostridium difficile. Эти бактерии в небольшом количестве содержатся в ЖКТ примерно у 3% населения.
Размножающиеся клостридии выделяют токсические вещества, оказывающие негативное влияние на слизистую оболочку кишечника и вызывающие развитие псевдомембранозного колита. Некоторые антибиотики усиливают повреждающее действие токсинов, что еще больше усугубляет возникшие нарушения. Стенка кишечника теряет свои барьерные свойства и начинает интенсивно секретировать жидкость в просвет кишки. Токсичные соединения всасываются в организм, вызывая развитие интоксикации. Жидкость перемещается в просвет кишечника, развивается обезвоживание, возникают электролитные расстройства.
В тяжелых случаях у больных псевдомембранозным колитом выявляются нарушения белкового обмена. Страдает сердечно-сосудистая система. Возможно формирование токсического мегаколона и прободение стенки кишечника с излитием кишечного содержимого в брюшную полость. Причиной летального исхода при псевдомембранозном колите может стать перитонит, обусловленный инфицированием брюшной полости микроорганизмами, содержащимися в каловых массах, или обезвоживание и нарушение функций различных органов и систем в результате интоксикации и грубых обменных расстройств.
Псевдомембранозный колит может рассматриваться, как внутрибольничная инфекция. Болезнь часто развивается при лечении в стационарных условиях, особенно – при пребывании в одной палате с пациентами, страдающими данной патологией. Факторами, увеличивающими вероятность развития псевдомембранозного колита и одновременно усугубляющими его течение, являются пожилой возраст, декомпенсированные соматические заболевания, болезни ЖКТ, бесконтрольный прием антацидов, почечная недостаточность, злокачественные опухоли, иммунные нарушения (в том числе – при СПИДе), ослабление организма после обширных хирургических вмешательств, а также состояния различного генеза, требующие проведения интенсивной терапии.
Симптомы колита
Клиническая картина псевдомембранозного колита определяется тяжестью патологии. При легких формах наблюдаются поносы и схваткообразные боли в животе на фоне ухудшения общего состояния организма. Стул обильный, водянистый, возможно – с примесями слизи. Общая интоксикация при псевдомембранозном колите проявляется в виде повышения температуры тела, слабости, разбитости, головной боли, тошноты и рвоты. Выраженность диареи и интоксикационного синдрома могут различаться. Все признаки исчезают после отмены антибиотиков.
При тяжелой форме болезни и псевдомембранозном колите средней степени тяжести клиническая симптоматика сохраняется в течение 1-2 и более недель после прекращения антибиотикотерапии. Пациенты страдают от изнуряющей диареи. Кал приобретает специфический вид «рисового отвара» желтоватой или зеленоватой окраски. В каловых массах больных псевдомембранозным колитом выявляются примеси слизи и крови. Потери значительных количеств жидкости с калом обуславливают развитие дегидратации и расстройств водно-электролитного обмена, проявляющихся слабостью, учащением пульса, снижением артериального давления, нарушением тонуса мышц и парестезиями. Возможны судороги. Отмечается уменьшение количества выделяемой мочи.
Отличительными особенностями тяжелой формы псевдомембранозного колита являются более бурное течение и появление крови в фекальных массах с первых дней заболевания. Наблюдается быстрое нарастание интоксикации, в сочетании с интенсивными схваткообразными болями в левой половине живота (преимущественно – в проекции сигмовидной кишки). Тяжелым осложнением псевдомембранозного колита может стать образование патологического расширения кишечника (мегаколона) с последующим разрывом кишки и развитием перитонита. О развитии мегаколона свидетельствует ухудшение состояние пациента с гипертермией до 39 градусов и выше в сочетании с уменьшением частоты дефекаций и увеличением объема живота.
У некоторых пациентов с псевдомембранозным колитом выявляется реактивный артрит. Иногда наблюдается экссудативная энтеропатия – невоспалительное поражение кишечника, сопровождающееся нарушениями белкового обмена и гипопротеиновыми отеками, обусловленными потерей большого количества белка через желудочно-кишечный тракт. Известны случаи стремительного развития псевдомембранозного колита с быстрым обезвоживанием, развитием гиперкалиемии и последующей остановкой сердца.
Диагностика
Диагноз устанавливается специалистом-проктологом или гастроэнтерологом с учетом анамнеза (прием антибиотиков или других препаратов, способных спровоцировать развитие заболевания), жалоб, данных физикального исследования и дополнительных диагностических процедур. В ходе внешнего осмотра больного псевдомембранозным колитом врач отмечает гипертермию, артериальную гипотонию, тахикардию, увеличение объема живота и болезненность при пальпации. В общем анализе крови определяется лейкоцитоз. При исследовании кала выявляются кровь и слизь. При бактериологическом исследовании фекальных масс обнаруживаются Clostridium difficile.
При проведении эндоскопического исследования у пациентов с псевдомембранозным колитом визуализируется слизистая оболочка, покрытая характерными желтоватыми фибринозными пленками (псевдомембранами). Обычно для подтверждения диагноза достаточно ректороманоскопии, поскольку псевдомембранозный колит чаще поражает дистальные отделы толстой кишки. В сомнительных случаях и при необходимости оценить состояние верхних отделов толстого кишечника проводят колоноскопию. При подозрении на развитие мегаколона назначают радиологические исследования (КТ, рентгенографию).
Лечение псевдомембранозного колита
Лечение данной патологии преимущественно консервативное. Больным отменяют антибиотики, назначают специальную диету, рекомендуют употреблять больше жидкости для предупреждения дегидратации. При легких формах псевдомембранозного колита этиотропные препараты обычно не требуются. При среднетяжелой и тяжелой форме болезни используют метронидазол. При наличии противопоказаний к применению данного препарата проводят терапию ванкомицином. Для восстановления нормальной микрофлоры кишечника назначают препараты бифидум и лактобактерий.
При тяжелых формах псевдомембранозного колита осуществляют инфузионную терапию для восстановления объема жидкости, устранения интоксикации, коррекции потерь белка и электролитных нарушений. При псевдомембранозном колите, осложненном токсическим мегаколоном, показано хирургическое вмешательство – сегментарная резекция пораженной части кишечника. Перфорация кишки является показанием к проведению неотложной операции – удалению пораженного отдела кишки, промыванию и дренированию брюшной полости для предупреждения развития перитонита.
Прогноз и профилактика
Прогноз при псевдомембранозном колите определяется тяжестью заболевания. Средняя вероятность гибели пациентов с данной патологией при отсутствии лечения составляет около 30%. При легких формах псевдомембранозного колита обычно наблюдается выздоровление после прекращения антибиотикотерапии. При колитах средней тяжести клиническая симптоматика сохраняется в течение нескольких недель, в последующем возможны рецидивы. Тяжелые формы псевдомембранозного колита часто завершаются гибелью пациентов. Шансы на благополучный исход при мегаколоне и перфорации кишечника еще больше снижаются, поскольку оперативные вмешательства приходится проводить в условиях резкого ослабления организма больного. Кроме того, перфорация толстой кишки часто осложняется перитонитом даже при раннем оперативном вмешательстве, что обусловлено наличием большого количества бактерий в кишечном содержимом.
Основной профилактической мерой является обоснованное назначение антибиотиков, выбранных с учетом индивидуальных противопоказаний, состояния больного и риска развития псевдомембранозного колита. Необходимо одновременное использование средств для предупреждения дисбактериоза, особенно – при продолжительной антибиотикотерапии. В группу высокого риска возникновения псевдомембранозного колита включают больных в возрасте старше 65 лет и пациентов, постоянно принимающих средства из группы антагонистов гистаминовых рецепторов. Больным из этой группы не рекомендуется назначать антибиотики, часто провоцирующие псевдомембранозный колит.
Псевдомембранозный колит — симптомы и лечение
Что такое псевдомембранозный колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Аверина Александра Анатольевича, гастроэнтеролога со стажем в 16 лет.
Над статьей доктора Аверина Александра Анатольевича работали литературный редактор Вера Васина , научный редактор Роман Васильев и шеф-редактор Маргарита Тихонова

Гастроэнтеролог Cтаж — 16 лет
Медицинский центр «Норма»
Дата публикации 24 января 2022 Обновлено 24 января 2022
Определение болезни. Причины заболевания
Псевдомембранозный колит (Pseudomembranous colitis) — это острое воспалительное заболевание толстого кишечника, вызываемое токсигенными штаммами бактерии Clostridium difficile [1] . Микроб вырабатывает токсины А и В, повреждающие кишечную стенку, и белок, угнетающий перистальтику кишечника. В результате возникает диарея, боль в животе, появляется слизь и иногда примесь крови в кале.
Характерным признаком заболевания являются фиброзные наложения на слизистой оболочке толстой кишки [27] [28] .
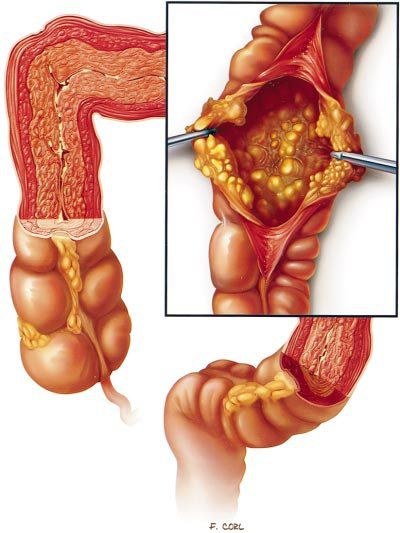
Псевдомембранозный колит (ПМК) чаще всего развивается после лечения антибиотиками. Его ещё называют Clostridium difficile-ассоциированным псевдомембранозным колитом, антибиотик-ассоциированным псевдомембранозным и клостридиозным колитом.
Эпидемиология
Заболеваемость ПМК лучше всего отслеживается в США и странах западной Европы [2] . В России статистический учёт заражения C. diff не ведётся. Согласно систематическому обзору за 2011 год, каждый 5-й случай из всех антибиотик-ассоциированных диарей (ААД) и каждый 2–3 случай внутрибольничной ААД в странах Европы и Северной Америки вызваны C. diff [3] .
В стационарах США среди внутрибольничных инфекций C. diff занимает первое место (12,1 % от общего количества), опережая K. pneumoniae (9, 7 %) и E. coli (9,3 %) [4] . В 2011 г. было зафиксировано более 450 тыс. случаев C. difficile-ассоциированной болезни и более 29 тыс. смертей от неё [29] .
В европейских странах заболеваемость C. diff составляет около 7 случаев на 10000 койко-дней, т. е. при средней госпитализации 10 дней, 7 случаев из 1000 госпитализаций заканчиваются ПМК. В 20 европейских странах это значение колеблется от 0,7 до 28,7 на 10000 койко-дней [5] .
В России в 2011 году было продано 295 млн упаковок антибиотиков, в 2019 — 379 млн [8] [26] . Антибактериальных препаратов потребляется всё больше, их продажа из аптек не контролируется, поэтому проблемы ААД и ПМК актуальны и в нашей стране.
В клиниках Санкт-Петербурга у пациентов с ААД тест на токсины C. diff был положительным в 47,7 % случаев [6] .
Смертность от ПМК колеблется от 9,3 до 22 % и зависит от возраста пациента, смерть чаще наступает при тяжёлом течении заболевания [7] [26] .
В настоящее время увеличилась внутри- и внебольничная заболеваемость C. difficile-ассоциированной болезнью, расширились группы риска, стали чаще встречаться рецидивы и тяжёлые формы, в том числе вызванные более патогенным штаммом BI/NAP1/027, возросла смертность [27] .
Причины псевдомембранозного колита
Основная причина болезни — это приём антибиотиков. ПМК могут вызывать любые антибактериальные препараты, но наиболее часто к нему приводит применение Клиндамицина, хинолонов, цефалоспоринов 2-го и 3-го поколения, карбапенемов. Реже ПМК развивается после приёма макролидов, пенициллина, Тетрациклина, Тигециклина.
К факторам риска, помимо приёма антибиотиков, относятся:
- возраст старше 65 лет;
- терапия ингибиторами протонной помпы и Н2-гистаминоблокаторами — препаратами, снижающими секрецию соляной кислоты в желудке;
- лечение в стационаре, особенно в отделениях реанимации, — каждые 7 дней госпитализации увеличивают риск ПМК на 8 % [1][9][10] ;
- наличие дополнительной патологии, в том числе воспалительных заболеваний кишечника, ВИЧ, сахарного диабета[31][32][33] ;
- хирургические вмешательства на органах ЖКТ;
- энтеральное питание, в том числе через назогастральный зонд;
- приём иммуносупрессивных препаратов (глюкокортикостероидов, Такролимуса) и противоопухолевых средств [31] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы псевдомембранозного колита
Наиболее частые симптомы лёгкого или умеренного псевдомембранозного колита:
- водянистая диарея (жидкие испражнения, похожие на кашицу) от трёх раз в сутки на протяжении двух и более дней в сочетании с болью в животе;
- лёгкие спазмы в животе, часто сопровождающиеся с позывами на стул, но не всегда приводящие к дефекации;
- примеси слизи, крови или гноя в испражнениях;
- температура тела 38,5 °С и более;
- тошнота или потеря аппетита.
При тяжёлом течении псевдомембранозного колита возникает водянистая диарея с кровью, уровень альбумина снижается менее 30 г/л, что сочетается с одним из следующих симптомов: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) и/или болезненностью при ощупывании живота. На фоне длительной диареи организм теряет много жидкости, что приводит к обезвоживанию и проявляется тёмно-жёлтой мочой, чувством жажды, усталости, головокружением, спутанностью сознания и заторможенностью [1] [9] .
При рецидиве болезни симптомы появляются повторно менее чем через 8 недель после окончания терапии.
Проявления псевдомембранозного колита схожи с симптомами других инфекций, поражающих толстый кишечник. Но в отличие от них признаки ПМК могут быть слабо выражены и, как правило, наблюдаются долго: от одной недели до нескольких месяцев. Также встречаются случаи, когда человек является носителем возбудителя ПМК — C. diff, но симптомы полностью отсутствуют.
Патогенез псевдомембранозного колита
В основе патогенеза ПМК лежит чрезмерное размножение бактерий C. diff на фоне уменьшения или гибели нормальной микробиоты толстого кишечника. C. diff вырабатывает токсины А и В, которые вызывают воспаление в кишечной стенке. На течение заболевания влияет состояние иммунной системы пациента и патогенные свойства бактерий, такие как вирулентность, наличие токсинов А и В.
Основной путь передачи инфекции — фекально-оральный. Бактерии попадают в организм с загрязнённых поверхностей, например с дверных ручек, смесителей, ручек смыва сливного бачка, мебели или медицинского инвентаря. Также переносить инфекцию может персонал больницы и заражённые пациенты.
Бактерии C.diff образуют споры, которые устойчивы к действию антибиотиков и могут длительно сохраняться в желудочно-кишечном тракте человека, заражая окружающих и вызывая рецидивы заболевания у самого пациента [12] .
Для некоторых людей C.diff — это часть нормальной микрофлоры ЖКТ, но в таком случае численность бактерий контролируется за счёт других микроорганизмов и работы иммунной системы.
Основные поражающие факторы C.diff — это выделяемые ею токсины [1] . Токсин А (энтеротоксин, белковая молекула с массой 308 кДа) влияет на секрецию жидкости, приводит к повреждению слизистой оболочки кишечника (мембран клеток) и вызывает воспалительный ответ со стороны иммунной системы.
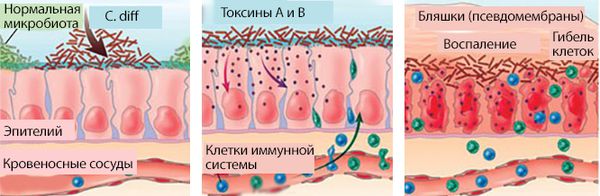
Токсин В (цитотоксин, белковая молекула с массой от 250 до 270 кДа) в 1000 раз более цитотоксичен по сравнению с токсином А. Он вызывает распад филаментного актина — белка, поддерживающего целостность клеток. В результате клетки слизистой разрушаются и гибнут. Токсин В опасен для человека, но не приводит к воспалению и повреждению слизистой оболочки кишечника у животных.
Под действием токсинов в кишечной стенке развивается специфическое воспаление с характерными изменениями на поверхности слизистой. Она становится отёчной, разрыхляется, приобретает ярко-красный цвет, на ней исчезает сосудистый рисунок. При контакте эндоскопа со слизистой капельки крови не появляются. Наблюдается множество желтовато-белых бляшек диаметром 3–5 мм, которые плотно фиксированы к слизистой оболочке. При взятии биопсии они отрываются с трудом, торцом эндоскопа не снимаются. Преобладает два типа воспалительных реакций: диффузно-катаральное воспаление слизистой и очаги фибриноидного некроза — бело-жёлтые бляшки, или псевдомембраны, поэтому такой тип колита называется псевдомембранозным.
![Бляшки при ПМК [35]](https://probolezny.ru/media/bolezny/psevdomembranoznyy-kolit/blyashki-pri-pmk-35_s.jpeg)
В биоптатах, полученных из воспалительно-изменённых участков слизистой, выявляют скопление иммунных клеток крови и слизистой, расширение капилляров и некроз клеток покровного эпителия [1] .
В биоптатах, взятых из бляшек, присутствует фибрин, обрывки некротизированного покровного эпителия, слизь, лейкоциты, плазматические клетки и колонии бактерий.
Чтобы определить патогенность клостридий, нужно выявить их токсины. Посев биоптатов на питательные среды удовлетворительных результатов не даёт. Метод в данном случае затратен и неинформативен, поэтому токсины C. diff определяют в кале.
Воспалительный процесс, как правило, захватывает несколько отделов толстого кишечника, но чаще поражена его прямая и сигмовидная часть, реже вовлекается вся толстая кишка. Протяжённость её поражения связана с тяжестью течения заболевания: чем больше толстого кишечника вовлечено в воспалительный процесс, тем тяжелее протекает колит и ярче симптомы.
Продолжительное воспаление в кишечной стенке приводит к следующим нарушениям:
- не всасывается жидкость, из-за чего развивается обезвоживание;
- потери крови из образующихся эрозий и язв приводят к анемии;
- кишечная стенка становится проницаемой для токсинов возбудителя и продуктов его жизнедеятельности, находящихся в просвете кишки, из-за чего нарастает общая интоксикация.
При тяжёлом течении прекращается перистальтика толстого кишечника, развивается токсический мегаколон и возникает полиорганная недостаточность, из-за чего пациент может погибнуть.
Классификация и стадии развития псевдомембранозного колита
ПМК входит в группу антибиотик-ассоциированных диарей. В Международной классификации болезней (МКБ-10) псевдомембранозный колит кодируется как АО 4.7 — Энтероколит, вызванный Clostridium difficile.
В зависимости от тяжести течения болезни и клинической картины выделяют следующие формы:
- ПМК лёгкой или умеренной тяжести. Проявляется диареей — неоформленным жидким, кашицеобразным стулом три или более раз в сутки и болью в животе.
- ПМК тяжёлого течения. Сопровождается водянистой диареей с кровью и изменениями в анализах. В биохимическом анализе крови отмечается низкий уровень альбумина (меньше 30 г/л), который сочетается с одним из следующих признаков: высоким уровнем лейкоцитов в клиническом анализе крови (> 15×10 9 /л) в клиническом анализе крови и/или болезненностью при ощупывании живота.
- Осложнённые формы ПМК. Протекают с водянистой диареей с кровью и одним из следующих симптомов: снижение артериального давления, температура тела ≥ 38,5 °C, отсутствие перистальтики тонкого кишечника, помрачение или угнетение сознания. В клиническом анализе крови лейкоциты повышены > 25×10 9 /л или снижены < 2×10 9 /л, возникает органная и почечная недостаточность, требуется искусственная вентиляция лёгких.
- Рецидивирующее течение ПМК. Заболевание развивается повторно менее чем через 8 недель после окончания терапии [1][14] .
Данная классификация используется для выбора схемы лечения.
Осложнения псевдомембранозного колита
Наиболее частые осложнения псевдомембранозного колита:
- Обезвоживание и электролитные нарушения — из-за сильной и длительной диареи нарушается ритм сердца, снижается артериальное давление и мышечный тонус. Чаще эти осложнения развиваются при недостаточном восполнении потерянной жидкости и солей.
- Почечная недостаточность — при стремительном обезвоживании нарушается работа почек, из-за чего снижается частота мочеиспусканий, появляются отёки, по анализам крови видно, что растёт содержание азотистых шлаков.
- Токсический мегаколон — расширение толстой кишки, редкое осложнение с плохим прогнозом. На фоне диареи частота стула резко урежается до одного раза в сутки, в дальнейшем дефекация прекращается полностью. Это происходит из-за замедления и полного прекращения перистальтики толстого кишечника. Из-за распирания толстого кишечника газами и содержимым нарастает вздутие живота, усиливается боль в нём. Интоксикация и электролитные нарушения приводят к резкому ухудшению самочувствия и выраженной слабости. В дальнейшем стенка кишки разрывается, содержимое изливается в брюшную полость (перфорация кишечника) и начинается перитонит. Как правило, это осложнение наблюдается у ослабленных пациентов, находящихся в отделении реанимации и хирургии.
- Перфорация кишечной стенки — образуется сквозное отверстие в кишечной стенке с излитием содержимого кишечника в брюшную полость и развитием перитонита.
- Полиорганная недостаточность — может привести к гибели пациента [1][15] .
Диагностика псевдомембранозного колита
Тесты на C. diff показаны при длительной диарее с болью в животе и/или примесью крови в стуле, возникшей спустя 3–60 суток после выписки из стационара и/или после приёма антибиотиков [1] .
Чтобы выявить токсигенные штаммы C. diff, токсины A и B определяют в кале [16] .
Для этого используют следующие методы:
- Цитотоксиновый копрологический тест. Чувствительность — 95 %, специфичность — 99 %, результат — в течение 2–3 дней.
- ELISA (Enzyme Linked Immuno Sorbent Assay) — фермент-связанный иммуносорбентный тест для определения токсинов. Чувствительность — 70–90 %, специфичность — 99 %, результат — через 4–6 часов.
- ПЦР (полимеразная цепная реакция) на токсин В. Чувствительность — 96 %, специфичность — 100 %, результат — в течение нескольких часов.
Чувствительность теста — это доля положительных результатов среди больных людей, т. е. вероятность правильно определить инфекцию у заболевших, отсутствие ложноотрицательных результатов. Специфичность — доля отрицательных результатов среди здоровых людей, т. е. отсутствие ложноположительных результатов.
Посев кала на C.diff не проводится, так как этим методом не удаётся определить токсигенные штаммы.
С помощью дополнительных методов можно оценить тяжесть состояния пациента и своевременно выявить осложнения.
К дополнительным обследованиям относятся:
- ректороманоскопия или сигмоидоскопия — позволяют обнаружить типичные изменения стенки кишки (множественные желтоватые бляшки 2–10 мм в диаметре, плотно фиксированные на поверхности слизистой оболочки);
- колоноскопия — помимо типичных изменений кишечной стенки, определяется распространённость процесса и поражение толстого кишечника выше сигмовидной кишки [17] ;
- обзорная рентгенография органов брюшной полости — используется, чтобы выявить признаки пареза кишечника и токсического расширения кишки;
- анализ крови — показывает уровень лейкоцитов (при ПМК повышен до 10–50 × 10 9 ), уровень креатинина (выше нормы) и альбумина (ниже нормы).
Гистологическое исследование биоптатов не является необходимым при C. difficile-ассоциированной болезни, но может быть крайне важным для дифференциальной диагностики.
Лечение псевдомембранозного колита
Методы лечения псевдомембранозного колита в российских и зарубежных клинических рекомендациях совпадают [1] [18] . При лёгком и среднетяжёлом течении его проводят в амбулаторных условиях (дома), при тяжёлом и/или осложнённом — в стационаре.
Для лечения ПМК назначаются антибиотики:
- Терапия первой линии — Метронидазол[19] . Препарат хорошо всасывается при приёме внутрь, применяется в течение 10 дней.
- Терапия второй линии — Ванкомицин. Применяется, если не эффективен Метронидазол и/или при тяжёлом течении заболевания. Плохо всасывается в кишечнике при приёме внутрь и оказывает преимущественно местное действие [20] . Курс также составляет 10 дней.
- Терапия резерва — Фидаксомицин, бактерицидный антибиотик группы макролидов местного действия, в России не зарегистрирован [21] .
- При осложнённом течении применяется комбинация Ванкомицин + Метронидазол. Лечение проводится в стационаре.
Антибиотики подавляют развитие C. diff. Бактерия чувствительна только к трём перечисленным антибактериальным препаратам.
При развитии осложнений ПМК могут применяться следующие методы:
- При токсическом мегаколоне показана колэктомия — удаление толстой кишки.
- Для лечения рецидивирующего ПМК в качестве экспериментального метода рассматривается трансплантация кишечной микробиоты (fecal microbiota transplantation, FMT) [23][24][25] . Кишечную микробиоту берут от здорового донора и при помощи назоинтестинального зонда, клизмы или колоноскопии переносят пациенту в кишечник. В России такое лечение считается экспериментальным. Проводится в научных клинических учреждениях, например в Федеральном научно-клиническом центре ФМБА России.
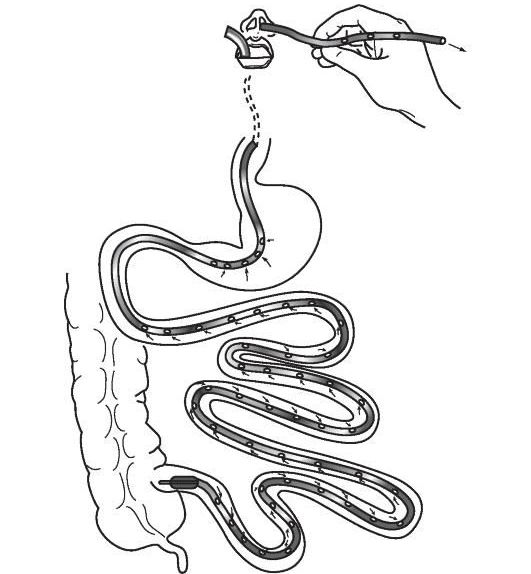
В качестве вспомогательных и симптоматических препаратов используются:
- Сорбенты (Диоктаэдрический смектит) — эффективно удаляет токсины C. diff, снижая их действие на кишечную стенку, улучшает качество стула.
- Пробиотики (Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium bifidum, Bifidobacterium infantis не менее 1×10 9 КОЕ/г) — подавляют активность C. diff. Данные об их эффективности пока противоречивы [22] .
- Препараты на основе дрожжей Saccharomyces cerevisiae (boulardii) — эффективны как вспомогательные и профилактические средства.
Прогноз. Профилактика
При лёгком или среднетяжёлом течении ПМК и хорошей реакции на стандартную терапию прогноз благоприятный, при тяжёлом и осложнённом — неблагоприятный. При рецидивирующем течении прогноз сомнительный, так как не разработаны эффективные схемы лечения.
Профилактика псевдомембранозного колита
Для профилактики развития ПМК следует:
- чаще мыть руки и соблюдать правила личной гигиены;
- рационально принимать антибиотики — строго по назначению врача с соблюдением всех указаний;
- изолировать пациентов с инфекцией C. diff в отдельные палаты, соблюдать меры санитарного режима;
- тщательно обрабатывать все поверхности хлорсодержащими или другими дезинфицирующими средствами, активными против спор C. diff;
- сокращать сроки госпитализации пациентов старше 65 лет [16] .
Чтобы предотвратить рецидив C. difficile-ассоциированной болезни, после завершения лечения Метронидазолом или Ванкомицином назначаются пробиотики курсом не менее трёх месяцев. Серьёзных побочных эффектов от них не выявлено [34] .
Список литературы
- Ивашкин В. Т., Ющук Н. Д., Маев И. В. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению Clostridium difficile-ассоциированной болезни // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2016. — № 5. — С. 56–65.
- Goudarzi M., Seyedjavadi S. S., Goudarzi H. et al. Clostridium difficile Infection: Epidemiology, Pathogenesis, Risk Factors, and Therapeutic Options // Scientifica (Cairo). — 2014.ссылка
- Nelson R. L., Kelsey P., Leeman H. et al. Antibiotic treatment for Clostridium difficile-associated diarrhea in adults // Cochrane Database Syst Rev. — 2011. — № 9.ссылка
- Magill S. S., Edwards J. R., Bamberg W. et al. Multistate Point-Prevalence Survey of Health Care–Associated Infections // N Engl J Med. — 2014. — № 13. — Р. 1198–1208. ссылка
- Davies K. A., Longshaw C. M., Davis G. L. et al. Underdiagnosis of Clostridium difficile across Europe: the European, multicentre, prospective, biannual, point-prevalence study of Clostridium difficile infection in hospitalised patients with diarrhoea (EUCLID) // Lancet Infect Dis. — 2014. — № 12. — Р. 1208–1219. ссылка
- Захарова Н. В., Филь Т. С. Микробиологические и клинические особенности инфекции Clostridium difficile // Инфекционные болезни. — 2015. — № 3. — С. 81–86.
- Lessa F. C., Winston L. G., McDonald L. C. et al. Emerging Infections Program C. difficile Surveillance Team. Burden of Clostridium difficile infection in the United States // N Engl J Med. — 2015. — № 24. — Р. 2369–2370. ссылка
- Анализ рынка антибиотиков в России в 2007–2011 гг, прогноз на 2012–2016 гг // BusinesStat. — 2012. — 82 c.
- Centers for Disease Control and Prevention. What is C. diff? — 2021. ссылка
- Hensgens M. P., Goorhuis A., Dekkers O. M. et al. Time interval of increased risk for Clostridium difficile infection after exposure to antibiotics // J Antimicrob Chemother. — 2012. — № 3. — Р. 742–748. ссылка
- Centers for Disease Control and Prevention. Vital Signs: Preventing Clostridium difficile Infections // Morbidity and Mortality Weekly Report (MMWR). — 2012. — № 9. — Р. 157–162. ссылка
- Surawicz C. M., Brandt L. J., Binion D. G. et al. Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections // Am J Gastroenterol. — 2013. — № 4. — Р. 478–498.ссылка
- Сотников В. Н., Разживина А. А., Веселов В. В. и др. Колоноскопия в диагностике заболеваний толстой кишки. — М: Экстрапринт, 2006. — 272 с.
- Шептулин А. А. Рефрактерные и рецидивирующие формы колита, ассоциированного с Clostridium difficile // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2011. — № 2. — С. 50–53.
- Mayo Clinic. Pseudomembranous colitis. — 2020.
- Planche T., Aghaizu A., Holliman R. Diagnosis of Clostridium difficile infection by toxin detection kits: a systematic review // Lancet Infect Dis. — 2008. — № 12. — Р. 777–784. ссылка
- Cerilli L. A., Greenson J. K. The differential diagnosis of colitis in endoscopic biopsy specimens: a review article // Arch Pathol Lab Med. — 2012. — № 8. — Р. 854–864.ссылка
- Рациональная фармакотерапия заболеваний органов пищеварения / под ред. В. Т. Ивашкина. — М.: Литтерра, 2011. — С. 522–526.
- Министерство здравоохранения РФ. Метронидазол: инструкция к по медицинскому применению лекарственного препарата. — 2021. — 9 с.
- Министерство здравоохранения РФ. Ванкомицин: инструкция к по медицинскому применению лекарственного препарата. — 2020. — 16 с.
- Fidaxomicin // Drugs in R&D. — 2010. — № 1. — Р. 37–45.ссылка
- Johnston B. C., Ma S. S., Goldenberg J. Z. et al. Probiotics for the prevention of Clostridium difficile-associated diarrhea: a systematic review and meta-analysis // Ann Intern Med. — 2012. — № 12. — Р. 878–888. ссылка
- Silverman M. S., Davis I., Pillai D. R. Success of self-administered home fecal transplantation for chronic Clostridium difficile infection // Clin Gastroenterol Hepatol. — 2010. — № 5. — Р. 471–473.ссылка
- Kleger A., Schnell J., Essig A. et al. Fecal transplant in refractory Clostridium difficile colitis // Dtsch Arztebl Int. — 2013. — № 7. — Р. 108–115.ссылка
- Шрайнер Е. В., Курилович С. А., Осипенко М. Ф. Трансплантация кишечной микробиоты: терапевтический потенциал при болезнях органов пищеварения // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2014. — № 5. — С. 63–68.
- Нечаева Ю. Обзор продаж антибактериальных препаратов по итогам 9 месяцев 2020 года // Ремедиум. — 2020. — № 10. — С. 18–21.
- Ивашкин В. Т., Шифрин О. С., Тертычный А. С. Clostridium difficile-ассоциированная болезнь // Росcийский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2015. — № 6. — С. 5–17.
- Шептулин А. А. Рефрактерные и рецидивирующие формы колита, ассоциированного с Clostridium difficile // Росcийский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2011. — № 2. — С. 50–53.
- Lessa F. C., Mu Y., Bamberg W. M. et al. Burden of Clostridium difficile infection in the united states // N Engl J Med. — 2015. — № 9. — Р. 825–834.ссылка
- Vecchio A. L., Zacur G. M. Clostridium difficile infection: an update on epidemiology, risk factors, and therapeutic options // Curr Opin Gastroenterol. — 2012. — № 1. — Р. 1–9. ссылка
- Furuya-Kanamori L., Stone J. C., Clark J. et al. Comorbidities, exposure to medications, and the risk of community-acquired Clostridium difficile infection: A systematic review and meta-analysis // Infect Control Hosp Epidemiol. — 2015. — № 2. — Р. 132–141. ссылка
- Haines C. F., Moore R. D., Bartlett J. G. et al. Clostridium difficile in a HIV-infected cohort: incidence, risk factors, and clinical outcomes // AIDS2013. — № 17. — Р. 2799–2807. ссылка
- Rodemann J. F., Dubberke E. R., Reske K. A. et al. Incidence of Clostridium difficile infection in inflammatory bowel disease // Clin Gastroenterol Hepatol. — 2007. — № 3. — Р. 339–344.ссылка
- Hempel S., Newberry S. J., Maher A. R. et al. Probiotics for the prevention and treatment of antibiotic-associated diarrhea: a systematic review and meta-analysis //JAMA. — 2012. — № 18. — Р. 1959–1969.ссылка
- Yu J. H., Kim N. Y., Lee H. M. et al. A case of pseudomembranous colitis in a juvenile rheumatoid arthritis patient taking methotrexate // Korean J Gastroenterol. — 2010. — № 6. — Р. 387–390. ссылка
Источник https://www.krasotaimedicina.ru/diseases/zabolevanija_proctology/pseudomembranous-colitis
Источник https://probolezny.ru/psevdomembranoznyy-kolit/
Источник